近日,桂林医科大学药学院李迎迎团队在化学类顶级期刊Journal of the American Chemical Society (IF = 15.6,中科院1区Top期刊)上发表了题为“A Heteroleptic/Trimetallic OsII–RuII–ZnII Sierpiński Triangle for Efficient Photodynamic Therapy of Hypoxic Tumors Mainly through Type I Mechanism”(https://doi.org/10.1021/jacs.5c07313)的研究文章。桂林医科大学药学院硕士研究生覃焕和广州大学硕士研究生陈帮塘、陈桥林为文章共同第一作者,桂林医科大学李迎迎副教授、蒋志敏副教授和广州大学蒋志龙副教授、王平山教授为共同通讯作者。

光动力疗法(PDT)利用光敏剂吸收光能,通过两种主要途径(I型和II型)产生活性氧(ROS)。在II型途径中,激发态光敏剂直接将能量传递给O2生成单线态氧(1O2),而在I型途径中,激发态光敏剂与周围底物发生复杂的电子转移,生成超氧阴离子自由基(O2−•)和羟基自由基(•OH)等。研究表明,II型PDT高度依赖于氧气的浓度,而I型PDT对氧气的依赖性较低,即使在低氧条件下仍能产生强的细胞毒性。然而,目前报道的大多数光敏剂都是通过II型途径产生1O2诱导肿瘤细胞死亡,这导致PDT治疗效果因肿瘤的缺氧微环境而大大降低。
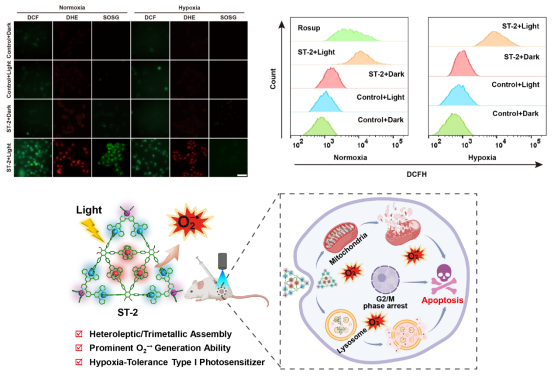
本研究通过配位驱动自组装构建了一种新型的杂配位OsII-RuII-ZnII Sierpiński三角形ST-2。出乎意料的是,具有独特结构的ST-2分子在光照下能够显著促进O2−•的产生,有利于I型PDT。在常氧和缺氧条件下,ST-2受光照后在细胞内均能高效产生O2−•,细胞内ROS清除实验表明O2−•对ST-2的光细胞毒性起主要作用,说明ST-2主要通过I型PDT诱导癌细胞死亡。在缺氧条件(1% O2)下,ST-2表现出非常出色的PDT性能,对4T1、MDA-MB-231、MCF-7、HeLa和A549细胞均具有极高的光毒性,IC50值在0.084−0.154 μM之间(亚nM范围),光毒性指数PI值高达750。进一步的研究证实,ST-2能够分解4T1细胞肿瘤球,有效抑制小鼠4T1肿瘤的生长,并具有良好的生物安全性。该项研究揭示了一种安全、高效的超分子配合物I型光敏剂及其光动力抗肿瘤作用,为开发基于超分子配合物的高效I型光敏剂提供了一种新的策略,并开辟了Sierpiński三角形在生物医学领域中的应用。
(文、图/ 李迎迎)